定期通信第18号では、5月31日に開催された平成25年度の講演会の聴講録を収載しました。
講演会では2名の演者の先生にご講演をいただいております。
講演の抄録、スライドハンドアウト、参考資料は「食の安全と微生物検査第3巻第1号」に特集として収載されています。会員の皆様には、参加された方は受付で配付させていただきましたが、欠席された方には事務局から送らせていただきました。特集をみながら定期通信をご覧いただきますと、ご理解いただき易いかと思います。会誌をお持ちでない方は、「発行された会誌の内容」に入手方法がございますので、是非ともご覧ください。
-
講演1:「新たな標準試験法の紹介1 黄色ブドウ球菌」
河野 潤一 先生 / 神戸大学大学院農学研究科資源生命科学専攻 感染症制御学 教授 -
講演2:「新たな標準試験法の紹介2 カンピロバクター」
百瀬 愛佳 先生 / 国立医薬品食品衛生研究所 食品衛生管理部 主任研究官
新たな標準試験法の紹介1 黄色ブドウ球菌
河野 潤一(神戸大学大学院農学研究科資源生命科学専攻 感染症制御学 教授)
重要な食中毒菌である黄色ブドウ球菌について、従来、我が国各検査機関で行われてきた方法論はまちまちであり、また問題点も指摘されてきた。さらに、食品流通がグローバル化されている現状では、検査法について得られる結果の解釈について国際的な互換性が確保されることが求められている。
そこで平成17~19年度にかけて行われた厚生労働科学研究(食の安心・安全確保推進事業)における分担研究「畜水産食品等の黄色ブドウ球菌の試験方法に関する研究」では、我が国と諸外国の検査法における各種の問題点を比較検討し、標準となる検査法の原案を作成した。その後「食品からの微生物検査標準法検討委員会」による詳細な検討を経て、黄色ブドウ球菌の試験法:直接平板培養法(NIHSJ-03-ST4)およびMPN法による菌数測定法(NIHSJ-05-ST4)が現在最終案として提示されている。その結論は以下のように要約される。
直接平板法培養法について、ISO68888-1との大きな違いは、国内慣行の卵黄加マンニット食塩培地がBaird-Parker培地に代替できるとした点である。他は基本的にISOに従うこととなっている。黄色ブドウ球菌の分離培地は国際的な協調の観点からは、諸外国で汎用されているBaird-Parker培地の使用が推奨されるところであるが、我が国では卵黄加マンニット食塩培地が従来から使用されてきた経緯がある。標準法の検討にあたっては、培地の性能比較を行い、加熱損傷菌に対してBaird-Parker培地が優れた発育能を有することが確認された。その他の試験では両培地間に、特段の発育能の差を認めなかった。したがって、加熱製品などで損傷菌の存在が予想される場合には、Baird-Parker培地の使用が強く推奨されるが、その他の場合には卵黄加マンニット食塩培地でも代替できるものとした。
増菌培養によるMPN法については、液体増菌培地の性能比較からISO68888-1のジオリッティカントー二(Giolitti and Cantoni)培地は採用しなかった。BAM(Bacteriological Analytical. Manual)の食塩・ピルビン酸Na添加TSBを採用したが、食塩濃度は10%ではなく、7.5%とした。最近、我が国では食塩やピルビン酸ナトリウムなどを添加した培地による選択増菌法が各機関で行われ、黄色ブドウ球菌検出率の著しい増加が報告されている。選択増菌培地を比較検討した結果、標準法で採用した培地は十分な性能を有し、国内での統一規格として十分と期待される。
新たな標準試験法の紹介2 カンピロバクター
百瀬 愛佳(国立医薬品食品衛生研究所 食品衛生管理部 主任研究官)
日本における食品の細菌学的試験は、規格基準が設けられているものは厚生労働省より発行される告示・通知が公定法として用いられている。また、規格基準が設けられていないものは日本食品衛生協会が刊行する食品衛生指針に則して試験が行われている。しかし、これらの検査法は策定過程が公開されておらず、また、定期的な見直し等が必ずしもされていないなどの問題点がある。このような背景から信頼性および実効性の双方の観点からガイドラインを示すことを目的として、2005年に「食品からの微生物標準試験法検討委員会」が立ち上げられた。
同委員会では、培養法を基準とした従来法の見直しや国際的に広く認められた試験法との整合性を考慮しながら、標準試験法の策定に向けた取り組みを行っている。
カンピロバクター
カンピロバクター食中毒は、事件数および患者数とも非常に多い細菌性食中毒であるが、カンピロバクターに関する食品の規格基準がないため、公定法に相当する試験法は規定されていない。カンピロバクターの分離培養は試験法によって検出結果が影響を受けやすいことが知られているため、前記の委員会において、国内で従来用いられてきた培地・培養条件、およびISO試験法(ISO 10272-1:2006)をもとに、カンピロバクター・ジェジュニ/コリ標準試験法(NIHSJ-02)の検討を重ねてきた。
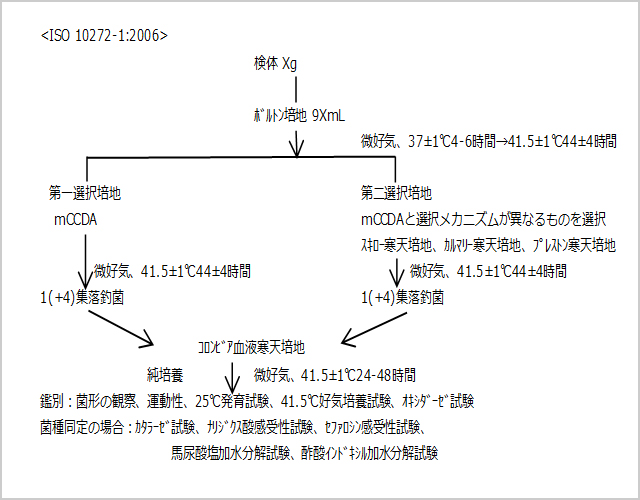
図1. ISO 10272-1:2006
ISO法では、損傷菌の回復を目的としてボルトン培地での37℃から41.5℃への温度シフトによる増菌法が用いられており、第一選択分離培地としてmCCDAを規定している。
しかし、近年、特に鶏肉での夾雑菌として基質拡張型β-ラクタマーゼ(ESBL)産生菌の検出の増加に伴い、ボルトン培地とmCCDAの組み合わせによるカンピロバクター分離成績の低下が指摘されている。そこで、NIHSJ-02案では、ESBL対策を目的としてプレストン培地を増菌培地として採用し、培養温度については、カンピロバクター属菌の中のジェジュニ/コリの検出を目的とすることより42℃を採用した。選択分離培地は第一選択分離培地をmCCDA、第二選択分離培地は試験所または試験者の判断で採用できることとした。
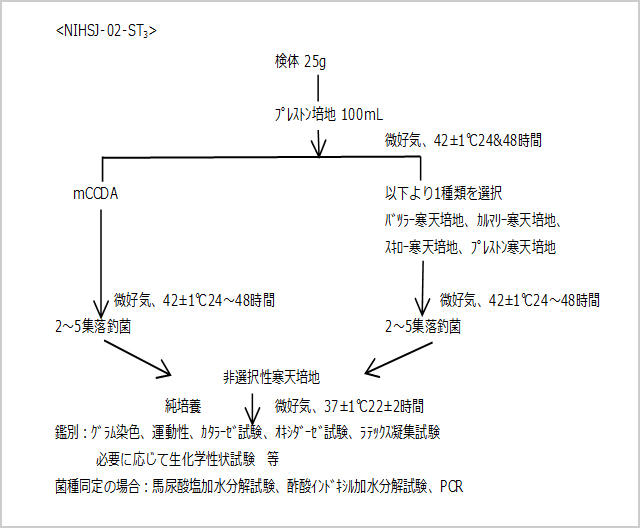
図2. NIHSJ-02-ST3
NIHSJ-02 最終案を確定させるため、損傷菌の回復とESBL対策のどちらを優先するのかについて結果を出すとともに、ISO法との整合性を比較するため、15機関によるCollaborative studyを実施し、NIHSJ-02案の妥当性の評価を行った。その結果、カンピロバクター・ジェジュニの検出感度において両法に有意差は認められなかったが、カンピロバクター・コリでは、NIHSJ-02案で検出率が高かった。夾雑菌の出現率はISO 10272-1:2006よりNIHSJ-02案の方が低い結果が得られた。このことから、NIHSJ-02はISO 10272-1:2006と比較して同等もしくはそれ以上の性能を有すると結論づけられた。
Collaborative studyの結果、Stage3を改良してStage4の最終案を確定し、標準試験法として公開にむけて準備中である。
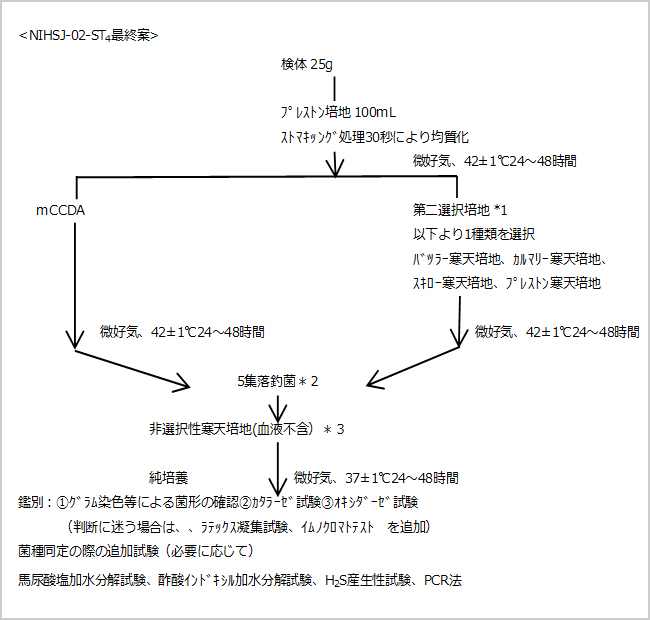
図3. NIHSJ-02-ST4最終案
*1)その試験法において共通に用いる、培地組成が明示された選択分離培地(ここではmCCDAを指す)に追加することによって、当該微生物の分離を補助する効果が期待できる選択分離培地。試験所または試験者が選択して用いることができる。
*2)5個釣菌した集落のうち、1個について鑑別同定を行う。カンピロバクター・ジェジュニ/コリと判定されなかった場合には、他の4個の集落について鑑別同定を行う。
*3)ブルセラ寒天培地 など
